
 研究責任医師(多施設共同研究の場合は研究代表医師)は、特定臨床研究の実施状況について※1年ごとに、
研究責任医師(多施設共同研究の場合は研究代表医師)は、特定臨床研究の実施状況について※1年ごとに、
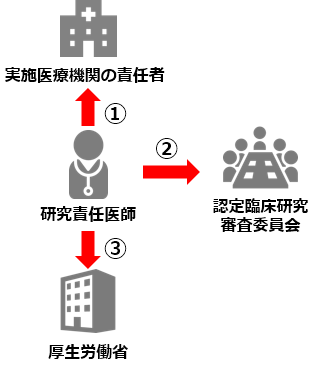
①実施医療機関の管理者に報告した上で、②認定臨床研究審査委員会へ報告することが定められています。
さらに認定臨床研究審査委員会が意見を述べた日から起算して1か月以内に③厚生労働大臣への報告を行なうことが義務付けられています。
| 報告先 | 報告事項 | 報告時期 |
|---|---|---|
| 認定臨床研究 審査委員会 |
|
実施計画を厚生労働大臣に提出した日(jRCT公表日)より、1年ごと、2か月以内に取りまとめて報告 例:公表日が2019年3月15日の場合、2019年3月15日~2020年3月14日の期間において実施状況を取りまとめ、2020年5月14日までに委員会へ報告を行う |
| 厚生労働大臣 |
|
認定臨床研究審査委員会が意見を述べた日から起算して1ヵ月以内 |
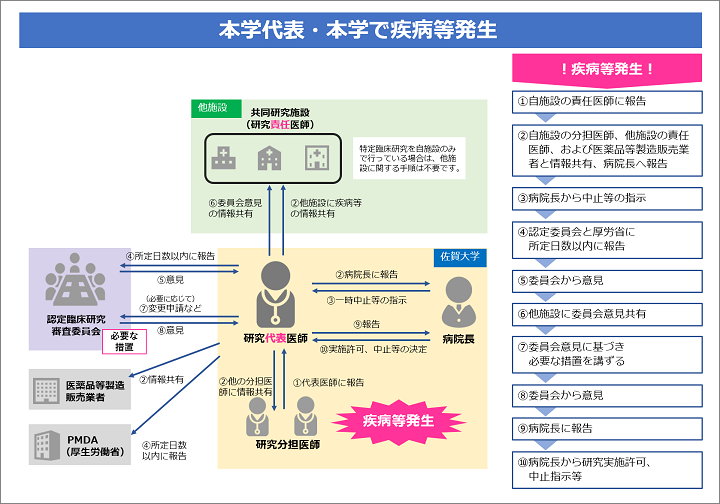
特定臨床研究の研究責任医師は、特定臨床研究の実施中に、下記の表に示す疾病等・不具合が発生した際に、実施医療機関の管理者および認定臨床研究審査委員会に報告することが臨床研究法により義務付けられています。
また、未承認・適応外の医薬品等の疾病等報告のうち、予期しない重篤なものについては、厚生労働大臣への報告も義務付けられており、jRCTのシステム内より行えます。
本学では、疾病等に該当しない重篤な有害事象(SAE)についても、実施医療機関の管理者および本学の認定臨床研究審査委員会に報告することが必要です。
※SAE報告の詳細は、こちらからダウンロードされる資料をご覧ください。
※当院の研究責任医師で判断に迷われる場合は、以下をご覧ください。
重篤な疾病等への対応
疾病等以外の重篤な有害事象への対応
|
PMDA |
委員会 |
定期報告 |
|||
|---|---|---|---|---|---|
|
医薬品等 |
未知 |
死亡 |
15日 |
○ |
|
|
重篤 |
15日 |
○ |
|||
|
非重篤 |
定期 |
○ |
|||
|
既知 |
死亡 |
15日 |
○ |
||
|
重篤 |
30日 |
○ |
|||
|
非重篤 |
定期 |
○ |
|||
|
感染症 |
未知 |
死亡・重篤 |
15日 |
○ |
|
|
非重篤 |
15日 |
○ |
|||
|
既知 |
死亡・重篤 |
15日 |
○ |
||
|
非重篤 |
定期 |
○ |
|||
|
不具合 (医療機器、 再生医療等製品) |
重篤(死亡含む)のおそれ |
30日 |
|||
|
未知 |
非重篤のおそれ |
||||
|
既知 |
非重篤のおそれ |
||||
|
PMDA |
委員会 |
定期報告 |
|||
|---|---|---|---|---|---|
|
医薬品等 |
未知 |
死亡・死亡のおそれ |
7日 |
7日 |
○ |
|
重篤 |
15日 |
15日 |
○ |
||
|
非重篤 |
定期 |
○ |
|||
|
既知 |
死亡・死亡のおそれ |
15日 |
○ |
||
|
重篤 |
定期 |
○ |
|||
|
非重篤 |
定期 |
○ |
|||
|
不具合 |
未知 |
死亡のおそれ |
30日 |
||
|
重篤のおそれ |
30日 |
||||
|
非重篤のおそれ |
|||||
|
既知 |
死亡のおそれ |
30日 |
|||
|
重篤のおそれ |
30日 |
||||
|
非重篤のおそれ |