
※新規申請書式一括ダウンロードはこちら
※新規申請書類チェックリスト(本学CRB提出用)
※臨床研究法による臨床研究実施手順書(佐賀大学版 研究者用)第7.0版
※臨床研究法上の臨床研究における疾病等に該当しない重篤な有害事象発生時の手順書 第1.0版
| 単施設の場合 | 多施設の場合 |
|---|---|
|
多施設共同研究の場合は、研究代表医師の指示に従って書類を作成してください。 |
書類提出先:crb@mail.admin.saga-u.ac.jp 提出期限:CRB開催の2ヶ月前
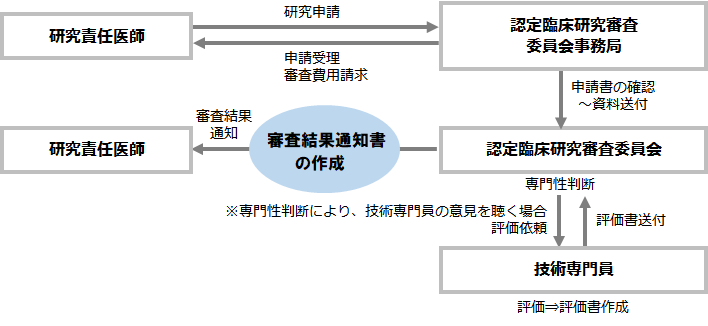


実施計画の提出方法
jRCTへの実施計画入力例(厚生労働省HPより)

| 実施計画提出の報告 | 計画変更 | 計画変更(軽微なもの) |
|---|---|---|
|
厚生労働大臣へ実施計画を提出し、jRCT公表後に報告。 実施医療機関の管理者へ報告CRBへ報告
|
CRBへの意見具申 厚生労働大臣へ届出 ★変更審査依頼書 |
変更後10日以内に CRBへ通知 厚生労働大臣へ届出 実施医療機関の管理者へ報告 ★軽微変更通知書 |
| 疾病等・不具合報告 重篤な有害事象(SAE)報告 |
不適合報告 重大な不適合報告 |
|---|---|
|
実施医療機関の管理者へ報告 ★医薬品の疾病等報告書 |
実施医療機関の管理者へ報告 (定期報告にてCRBへ報告) ★不適合報告書 重大な不適合の場合、 ★重大な不適合報告書 |
| モニタリング・監査 | 定期報告 |
|---|---|
|
(定期報告にてCRBへ報告) モニタリングの実施 |
定期報告(1回/年)は、実施計画を厚生労働大臣へ提出した日より、1年毎に実施状況を取りまとめ、2か月以内にCRBへ報告。 実施医療機関の管理者へ報告 ★定期報告書(CRB用) |
★は提出書類 詳細な手順については、臨床研究法による臨床研究実施手順書(佐賀大学版 研究者用)、
臨床研究法上の臨床研究における疾病等に該当しない重篤な有害事象発生時の手順書をご参照ください。
| 主要評価項目報告 | 中止報告 | 終了報告 |
|---|---|---|
| ◎主要評価項目報告書のデータベース記録・公表 ※主要評価項目に係るデータ収集終了から1年以内に作成し、その後遅滞なく実施医療機関の管理者へ提出。
|
研究計画書の中止基準に従い中止した日から、10日以内にCRBへ通知、厚生労働大臣へ届出 ※中止届を提出した場合でも、臨床研究終了までの間、疾病等報告、定期報告等を行うこと。 ★実施計画 |
◎総括報告書概要のデータベース記録・公表 ※全ての評価項目に係るデータ収集終了から1年以内に作成し、その後遅滞なく実施医療機関の管理者へ提出。 ★終了通知書 |